2021年3月16日
国立研究開発法人 国立精神・神経医療研究センター(NCNP)
国立大学法人 大阪大学
国立大学法人 筑波大学
国立研究開発法人日本医療研究開発機構(AMED)
印刷用PDF(1.2MB)
老いた脳の修復力を回復させるメカニズムを発見
【研究成果のポイント】
- 加齢により衰えた、脳の神経回路の修復力を回復させるメカニズムを発見しました。
- APJ受容体※1の活性化により、脳内の組織幹細胞、オリゴデンドロサイトの発達が促進されることを明らかにしました。
- APJ受容体の活性化による神経回路の修復促進が、多発性硬化症などの疾患に対する治療に有効である可能性が示されました。
概要
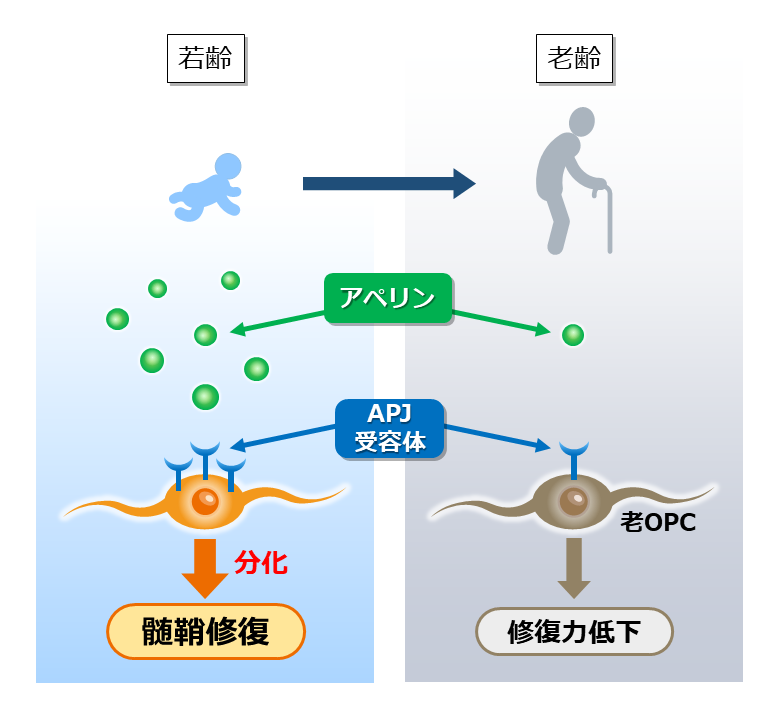
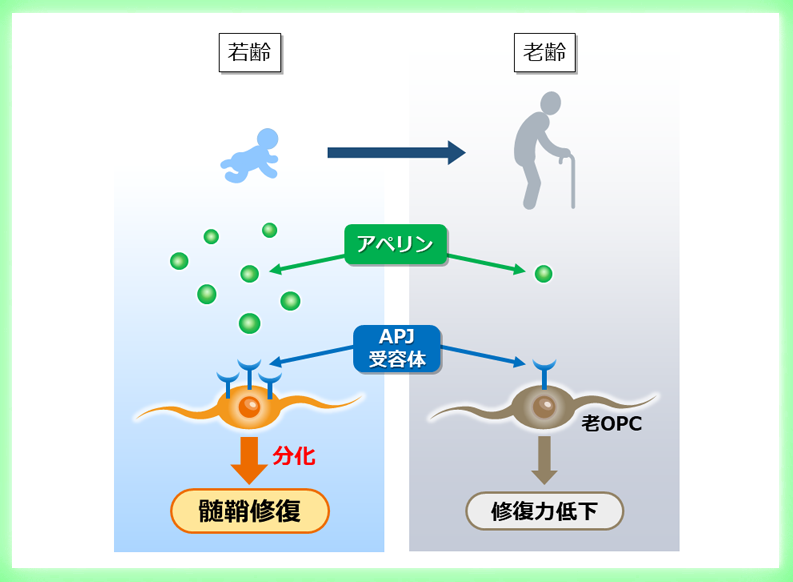
国立精神・神経医療研究センター(NCNP)神経研究所の村松里衣子部長(神経薬理研究部)らの研究グループは、大阪大学大学院医学系研究科の山下俊英教授、筑波大学生存ダイナミクス研究センター深水昭吉教授らと共同で、加齢に伴って低下した脳の修復力が、APJ受容体の働きによって回復することを明らかにしました(図1)。
様々な脳脊髄疾患で、脳や脊髄の神経回路が傷つきますが、傷ついた神経回路はしばしば自然に修復します。ところが加齢に伴い、神経回路は修復しにくくなります。その原因の一つに、神経回路そのものの修復能力の劣化が指摘されていますが、その分子メカニズムは十分解明されていませんでした。
今回、研究グループは、アペリン※2(Apelin)とAPJ受容体の働きによって、脳や脊髄の神経回路を構成する髄鞘※3という構造が修復することを発見しました。髄鞘の脱落は、指定難病の多発性硬化症※4などの病変に認められる特徴であり、健常な高齢者の脳でも観察される変化で、病態や老化による神経機能との関連が指摘されています。本研究成果から、APJ受容体の活性化が高齢者の脳機能の向上や多発性硬化症などの疾患の治療に有効である可能性が考えられます。
本研究成果は、米国科学誌「Nature Aging」に、米国東部時間(夏時間)2021年3月15日(月)12時(日本時間2021年3月16日1時)に公開されました。
研究の背景
髄鞘は神経機能の発揮に重要な役割を担う構造物です。髄鞘の修復には、オリゴデンドロサイト前駆細胞※5を分化させる必要がありますが、加齢にともない自然に分化することが難しくなります。加齢に伴うオリゴデンドロサイトの分化能力の低下には、オリゴデンドロサイト内の分子発現の変化が関わると報告されていましたが、キーとなる分子はわかっていませんでした。
研究の概要
研究グループは、マウスを用いた実験から、髄鞘が修復しやすい条件のオリゴデンドロサイトに豊富に発現する分子として、APJ受容体を見出しました。オリゴデンドロサイトに発現するAPJ受容体を欠損したマウスでは、髄鞘形成や運動機能の不良が顕著でした(図2)。
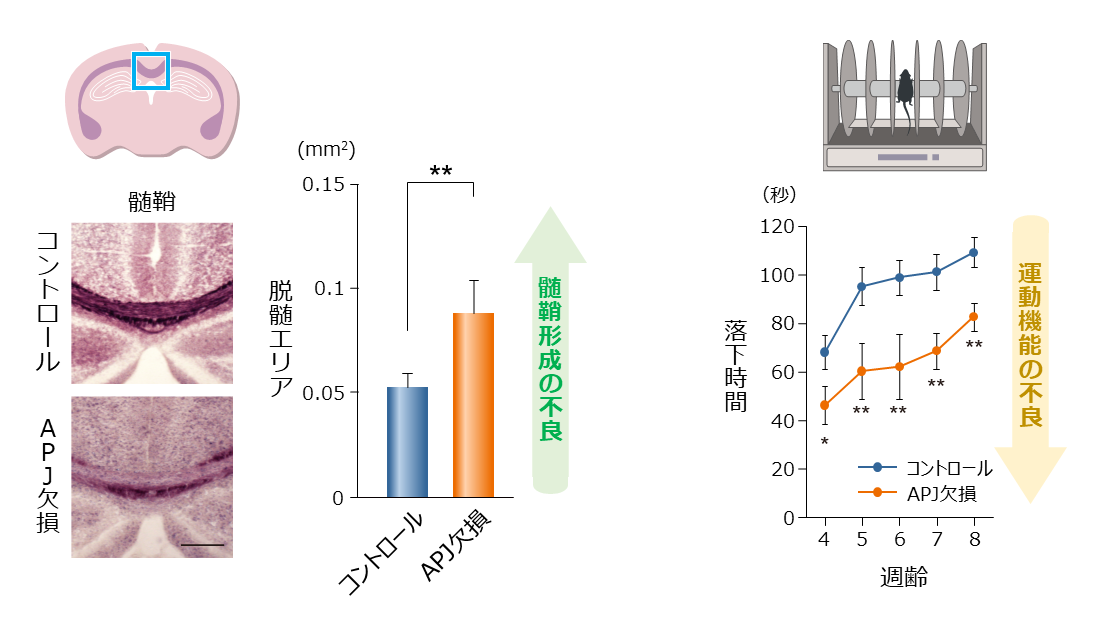
図2. APJ受容体欠損マウスでの髄鞘形成と運動機能の不良
また、老齢マウスを用いた実験から、老齢マウスでは体内のapelin量が低下していること、APJ受容体を活性化させると傷ついた髄鞘の修復が促進されることを突き止めました(図3)。さらに、多発性硬化症患者の脳内のオリゴデンドロサイトにもAPJ受容体が発現していること、また、培養細胞を用いた実験から、APJ受容体の活性化がヒトのオリゴデンドロサイトの分化も促すことを見出しました。
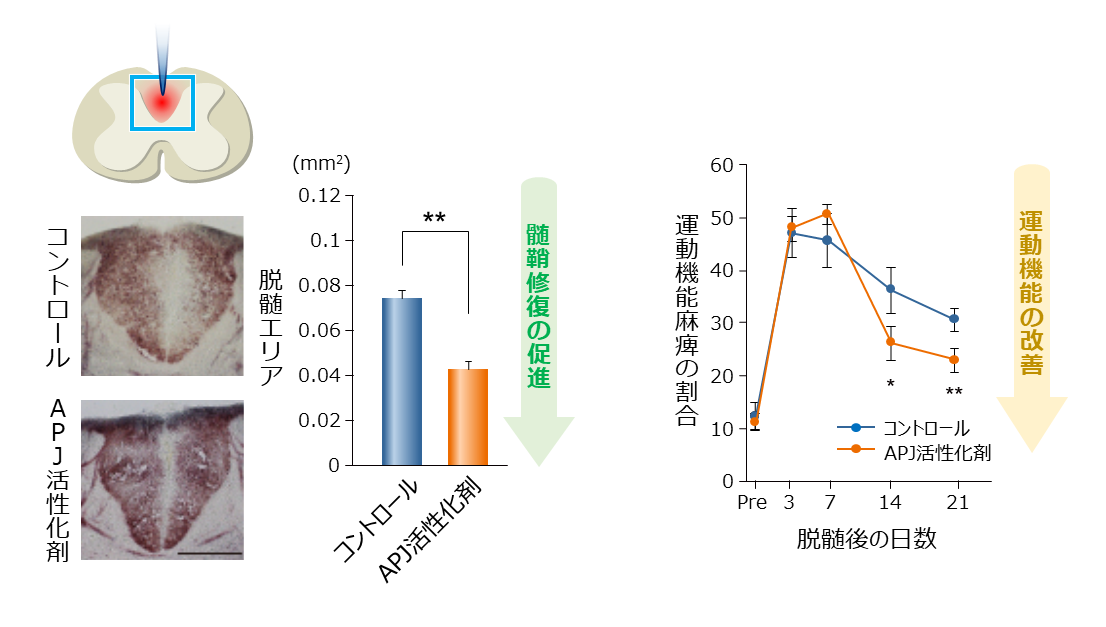
図3. APJ活性化剤による老齢脱髄マウスでの髄鞘修復・運動機能の改善効果
今後の展望
本成果により、老化脳を修復させるメカニズムの一端がわかりました。今後、apelinとAPJ受容体がどのような脳機能の改善作用を持つかについて更に研究を進めることにより、多発性硬化症など、髄鞘の傷害が見られる疾患に対する治療薬の開発につながることが期待されます。
用語の説明
1)APJ受容体
脳や血管内皮細胞など全身に広く発現する受容体。APJ受容体の内因性のリガンドの一つとして、アペリンが報告されている。
2)アペリン
様々な臓器から産生される生理活性ペプチド。これまでに、心血管機能や筋機能との関連が知られている。
3)髄鞘
神経活動の伝達に関わる構造物。脳や脊髄の様々な疾患の病変で、髄鞘の脱落が観察される。髄鞘が脱落した部位が担っていた神経機能が障害されるため、髄鞘の脱落が関わる疾患の症状の悪化と関連すると認識されている。
4)多発性硬化症
希少疾患で、難病指定されている。免疫系の異常により髄鞘が傷つくと考えられている。現時点で、髄鞘を修復させる治療薬はない。
5)オリゴデンドロサイト
髄鞘を構成する細胞で、脳内のグリア細胞の一種である。オリゴデンドロサイトの前駆細胞は脳や脊髄の広い範囲に存在している。
原著論文情報
・雑誌名:Nature Aging
・論文タイトル:
Age-dependent decline in remyelination capacity is mediated by apelin–APJ signaling
・著者:
Masumi Ito, Rieko Muramatsu†, Yuki Kato, Bikram Sharma, Akiko Uyeda, Shogo Tanabe, Harutoshi Fujimura, Hiroyasu Kidoya, Nobuyuki Takakura, Yukio Kawahara, Masaki Takao, Hideki Mochizuki, Akiyoshi Fukamizu, Toshihide Yamashita
(†責任著者)
・DOI:10.1038/s43587-021-00041-7
研究経費
本研究は日本学術振興会・科学研究費補助金基盤研究(19H03554, 17H06178)や、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(PRIME)「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」研究開発領域における研究開発課題「劣化した神経組織修復システムの復旧」(研究開発代表者:村松里衣子)の支援を受けて行われました。
お問い合わせ先
【研究に関するお問い合わせ】
国立精神・神経医療研究センター
神経研究所 神経薬理研究部
村松 里衣子
〒187-8502 東京都小平市小川東町4-1-1
042-346-1725
Email: muramatsu(a)ncnp.go.jp
【報道に関するお問い合わせ】
国立精神・神経医療研究センター 総務課広報係
〒187-8551 東京都小平市小川東町4-1-1
TEL: 042-341-2711(代表) FAX:042-344-6745
E-mail: ncnp-kouhou(a)ncnp.go.jp
大阪大学 大学院医学系研究科 広報室
〒565-0871 大阪府吹田市山田丘2-2
TEL: 06-6879-3388 FAX: 06-6879-3399
E-mail: medpr(a)office.med.osaka-u.ac.jp
筑波大学 広報室
〒305-8577 茨城県つくば市天王台1-1-1
TEL: 029-853-2040 FAX:029-853-2014
E-mail: kohositu(a)un.tsukuba.ac.jp
【AMEDに関するお問い合わせ】
国立研究開発法人日本医療研究開発機構 (AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課
〒100-0004 東京都千代田区大手町 1-7-1
Tel:03-6870-2224 Fax: 03-6870-2246
Email: kenkyuk-ask(a)amed.go.jp
※E-mailは上記アドレス(a)の部分を@に変えてご使用ください。