筋疾患診断支援事業における検査依頼機関の位置づけ
本事業は、『人を対象とする生命科学・医学系研究に関する倫理指針』(2021年6月30日施行)に準拠すべく、検査依頼機関を「研究協力機関」と位置づけています。
1)概要
本事業で提供する各種解析・検査は改正医療法(2018年12月1日施行)等で定めるところの検査とは異なり、担当医の診断支援目的として実施するものであり、広義の診療と位置づけています。しかし、検査後の検体を、将来的な研究利用の可能性を踏まえて「筋レポジトリー」として保管することから、『人を対象とする生命科学・医学系研究に関する倫理指針』(2021年6月30日施行)に準拠し、当センター倫理委員会にて承認(倫理承認番号:B2024-130)を得ています。
当該申請においては、検査依頼機関を「研究協力機関」と位置づけています(下図)。 研究協力機関での倫理審査は不要ですが、担当医から当該機関の施設長への報告が必要です(手続きについては、自施設の倫理委員会にお問い合わせください)。
当センターでの倫理委員会承認通知書ならびに事業計画書が必要となる場合には、当該青字部分をクリックしてダウンロードしてください。なお、当センターでは、研究協力機関の一覧を、当センター倫理委員会に提出しており、更に毎年、年度開始の一定期間内に、前年度の新規研究協力施設の一覧を提出します。
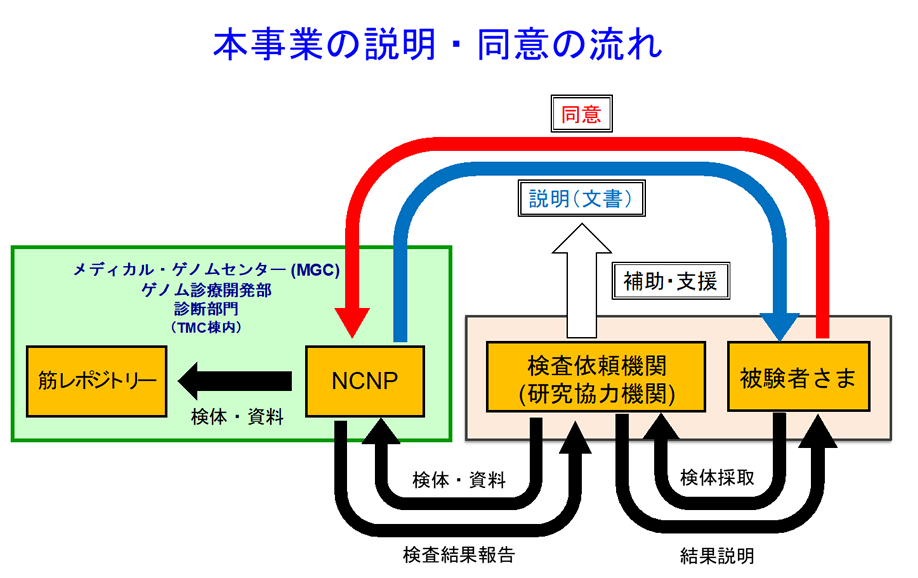
2) インフォームド・コンセント
本事業への同意取得は、当センターが用意した説明文書・同意文書によって行います。研究協力機関の担当医は、被験者が適切に本事業内容を理解できるように適宜支援を行い、記入済みの同意文書を検体・病歴などの資料とともにMGC検体受付窓口宛にご送付ください。なお、被験者への説明文書、および、疾病研究第一部のHP(https://www.ncnp.go.jp/nin/guide/r1/patients.html)には、本事業の説明を掲載するとともに、質問がある場合には問い合わせができるよう、連絡先およびメールアドレスを記載していますので、不明な点がある場合はご連絡ください。
3) 被験者への結果説明
解析結果は、同意取得支援を行った担当医に報告します。担当医は、医療の一環として結果を被験者にお伝えください。
4) 本事業に関する情報公開
本事業の公告文書については、以下のホームページ上に掲載しています。